2020年11月02日
反応前後で質量は変化しない!
こんにちは、YOSHIOです。
今回は化学変化の7回目、化学変化の質量です。
前回までに様々な化学変化を取り上げましたが、
今回は化学変化の前後における
質量の変化についてまとめていきます。
…ひょっとすると、中2化学分野で、
ブログ容量が最小になるかも…。
目で見て分かるように、
下図を準備しました。
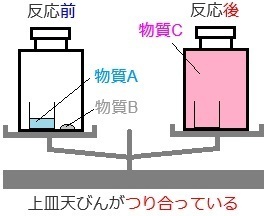
質量が同じ密閉容器内に、
左側:反応前の物質Aと物質B
右側:物質Aと物質Bが反応してできた物質C
という状態です。
※ 今回は、物質A=液体、
物質B=固体、物質C=気体の設定です。
そこで、
もし、左側の反応前の状態と、
右側の反応後の状態で、
質量を比べたとしたら…
実は、質量は等しい状態になります。
(上図でいう、つり合っている状態)
このように、化学変化の前後に関係なく、
質量が等しい関係を、
質量保存の法則といいます。
理科分野で質量と言えば、
計算を思い浮かべる人も多いと思います。
理科での質量計算は、
特別な条件や断りがない限りは、
質量保存の法則に従って計算することになります。
ちなみに、高校化学も同様になるので、
変に、
「密閉容器とか言いながら、
ふたが少し緩んでいるんじゃ…?」
や
「混ぜている時に量がピッタリじゃないかも…?」
などのような勘繰りはダメですよ。
(ウソのような本当の話で、
塾生の中でミス時にこの言い訳が実際にありまして…)
この質量保存の法則を使った計算を、
次回以降から扱うことになります。
ただ、身構えることはないので、
今回の重要ポイントだけを覚えてくださいね。
では、今回の化学変化の質量のポイントは2つ。
① 質量保存の法則は、化学変化前後で質量が変わらない
② 質量保存の法則は、今後の化学計算で重要な考え方
…実質暗記することは、①だけです。
具体的に、どのように計算に活かすかは、
次回からコツコツ頑張ってみましょうね。
化学変化の質量関係に注意して、
次回以降の質量計算、頑張ってみませんか?
≪コメント記入≫
感想や質問など、気軽にコメントしてOKです。
・お名前:ペンネームでOK
・コメント
を記入するだけで構いませんからね。
今回は化学変化の7回目、化学変化の質量です。
前回までに様々な化学変化を取り上げましたが、
今回は化学変化の前後における
質量の変化についてまとめていきます。
…ひょっとすると、中2化学分野で、
ブログ容量が最小になるかも…。
目で見て分かるように、
下図を準備しました。

質量が同じ密閉容器内に、
左側:反応前の物質Aと物質B
右側:物質Aと物質Bが反応してできた物質C
という状態です。
※ 今回は、物質A=液体、
物質B=固体、物質C=気体の設定です。
そこで、
もし、左側の反応前の状態と、
右側の反応後の状態で、
質量を比べたとしたら…
実は、質量は等しい状態になります。
(上図でいう、つり合っている状態)
このように、化学変化の前後に関係なく、
質量が等しい関係を、
質量保存の法則といいます。
理科分野で質量と言えば、
計算を思い浮かべる人も多いと思います。
理科での質量計算は、
特別な条件や断りがない限りは、
質量保存の法則に従って計算することになります。
ちなみに、高校化学も同様になるので、
変に、
「密閉容器とか言いながら、
ふたが少し緩んでいるんじゃ…?」
や
「混ぜている時に量がピッタリじゃないかも…?」
などのような勘繰りはダメですよ。
(ウソのような本当の話で、
塾生の中でミス時にこの言い訳が実際にありまして…)
この質量保存の法則を使った計算を、
次回以降から扱うことになります。
ただ、身構えることはないので、
今回の重要ポイントだけを覚えてくださいね。
では、今回の化学変化の質量のポイントは2つ。
① 質量保存の法則は、化学変化前後で質量が変わらない
② 質量保存の法則は、今後の化学計算で重要な考え方
…実質暗記することは、①だけです。
具体的に、どのように計算に活かすかは、
次回からコツコツ頑張ってみましょうね。
化学変化の質量関係に注意して、
次回以降の質量計算、頑張ってみませんか?
≪コメント記入≫
感想や質問など、気軽にコメントしてOKです。
・お名前:ペンネームでOK
・コメント
を記入するだけで構いませんからね。
【このカテゴリーの最新記事】
-
no image
この記事へのコメント
コメントを書く
この記事へのトラックバックURL
https://fanblogs.jp/tb/10311956
※ブログオーナーが承認したトラックバックのみ表示されます。
この記事へのトラックバック