2019�N01��19��
���A�t���C���ƌ������t�����s���ł��I
���A�t���C���ƌ������t�����s���ł��I
��5��@���A�a���҂ƃt���C���EADL�y����ғ��A�a�f�ẪR�c�z
CareNet ���J���F2019/01/15
�r�� �� ( ���炫 ���� ) ��
�����s���N������ÃZ���^�[ ���A�a�E��ӁE��������� ���ȑ�������
J-CLEAR�]�c��
Q1 ���ہA���A�a���҂łǂ̂悤�Ƀt���C����]�����܂����H
����A�a���҂ł̓t���C���E�T���R�y�j�A�A��i�I/��{�IADL�A���́A���͂Ȃǂ̐g�̋@�\��]�����邱�Ƃ���ł��B
���̒��ŁA�t���C���͗v���ɂȂ邱�Ƃ�h���Ƃ����Ӗ��ŏd�v�ȕ]�����ڂ�1�ł��傤�B
�t���C���͉���ɔ����ė\���\���ቺ���A�X�g���X�ɂ���ėv���⎀�S�Ɋׂ�₷����Ԃƒ�`����܂��i�}�P�j�B
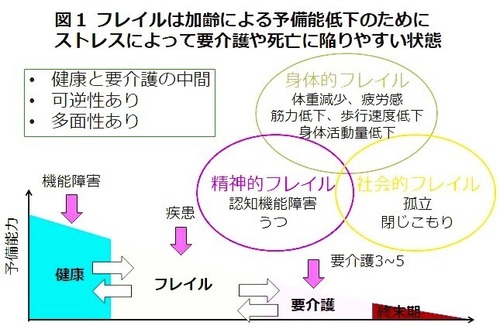
�{�M�ł̓t���C���͌��N�Ɨv���̒��Ԃ̏�ԂƂ���Ă��܂����A�C�O�ł͗v�����܂ޏꍇ������܂��B
�^����H������ɂ���Ĉꕔ���N�ȏ�Ԃɖ߂�ꍇ������Ƃ����t�����A�t���C���̓����ł��B
����1�̑傫�ȓ����͑��ʐ��ŁA�g�̓I�t���C�������łȂ��A�F�m�@�\�ቺ�₤�Ȃǂ̐��_�E�S���I�t���C���A��������Ȃǂ̎Љ�I�t���C�����܂߂��L���Ӗ��ŁA�t���C����]�����邱�Ƃ���ł��B
�t���C���ɂ͂��܂��܂Ȏw�W������܂����A�����ł͑傫�������ĂR�̃^�C�v���Љ�܂��B
1�ڂ͐g�̓I�t���C���ŁA�]���@�Ƃ���CHS�������܂��B
���̊��L.P.Fried�炪�������̂ŁA�̏d�����A��J���A�ؗ͒ቺ�A�g�̊����ʒቺ�A���s���x�ቺ��5���ڂ̂���3���ڈȏ㓖�Ă͂܂�ꍇ���t���C���Ƃ��܂��B
�̏d�����͒�h�{�A�ؗ͒ቺ�ƕ��s���x�ቺ�̓T���R�y�j�A�̏Ǐ�Ȃ̂ŁAFried��ɂ��g�̓I�t���C���́A��h�{��T���R�y�j�A���܂ފT�O�Ƃ������܂��B
�{�M�ł�CHS��̂��ꂼ��̍��ڂ̃J�b�g�I�t�l�⎿����C������J-CHS�������܂��i�\�P�j�B

2�ڂ�deficit accumulation model�i��Q�~�σ��f��)�ɂ��t���C���ŁA����҂ɑ����@�\��Q�⎾���̏W�ςɂ���Ē�`����܂��B
36���ڂ���Ȃ�Frailty Index����\�I�Ȋ�ł��B
��Q�������d�Ȃ邱�Ƃŗ\���\���ቺ���A���S�̃��X�N���傫���Ȃ�Ƃ����l���Ɋ�Â��č쐬����Ă��܂����A���ڐ��������A�Տ��I�Ɏg���ɂ����̂�����ł��B
3�ڂ͍���ґ����@�\�]���iCGA�j�Ɋ�Â����t���C���ł���A�g�̋@�\�A�F�m�@�\�A����ԁA��h�{�Ȃǂ𑍍��I�ɕ]���������ʂɊ�Â��ĕ]��������̂ł��B
�{�M�ł͉��\�h���f�Ŏg�p����Ă���u��{�`�F�b�N���X�g�v��CGA�Ɋ�Â����t���C���Ƃ�����ł��傤�B
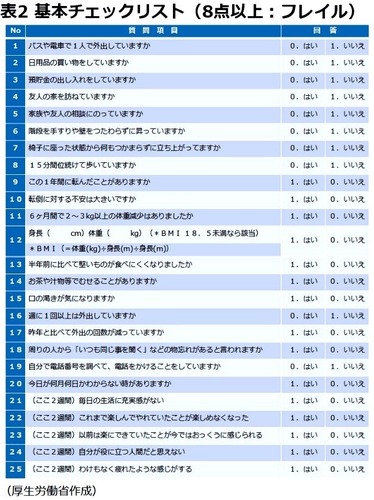
ADL�A�T���R�y�j�A�֘A�A��h�{�A���o�@�\�A��������A�F�m�A���Ȃǂ�25���ڂ�]�����A8���ڈȏ㓖�Ă͂܂�ꍇ���t���C���Ƃ��܂�1)�i�\�Q�j�B
�O���ʉ@�̍���A�a���҂ł܂��ȒP�Ɏ��{�ł���̂�J-CHS�ł��傤�B
��{�`�F�b�N���X�g���s�����Ƃ��ł���A�L���Ӗ��Ńt���C���̕]�����ł��܂��B
��{�`�F�b�N���X�g���s���̂�����ꍇ�ɂ�DASC-8���s���āA�i����ғ��A�a�̌����R���g���[���ڕW�ɂ�����j�J�e�S���[II�̊��҂�ΏۂɃt���C������s���Ƃ������@������܂��B
Q2 ���A�a�ƃt���C���EADL�ቺ�̊W�A�댯���q�́H
���A�a���҂́A����҂����łȂ����N�҂ł��t���C�����������₷�����Ƃ��킩���Ă��܂��B
���A�a���Ȃ��l�Ɣ�ׂāA���A�a���҂ł̓t���C���̃��X�N����5�{�A�v���t���C���̃��X�N����2.3�{�ƕ���Ă��܂�2)�B�܂��A���A�a���҂ł͎�i�IADL�ቺ��1.65�{�A��{�IADL�ቺ��1.82�{�������₷���Ƃ������^��͌��ʂ�����܂�3)�B
����A�a���҂ł́A���ɍ������A�d�ǒጌ���A�����d���������̍������t���C���̊댯���q�Ƃ��ďd�v�ł��BHbA1c 8.0���ȏ�̊��҂̓t���C���A���s���x�ቺ�A�]�|�A���܂��N�����₷���Ȃ�܂��i�}�Q�j�B
![�}2�������̓t���C���]�|����.jpg](/mappei/file/E59BB32E9AB98E8A180E7B396E381AFE38395E383ACE382A4E383ABE8BBA2E58092E9AAA8E68A98-thumbnail2.jpg)
������d�v�Ȃ��Ƃ́A���A�a�Ƀt���C������������Ǝ��S���X�N���傫���Ȃ邱�Ƃł��B
�_�������ďd�Ǔx���]���ł���t���C���ł́A�t���C�����d�ǂł���قǎ��S�̃��X�N�����܂邱�Ƃ��킩���Ă��܂��B
�p���̒����ł́A���A�a�Ƀt���C���������������҂ł͕��ϗ]���i�����l�j��23�����Ƃ����A�ɒ[�ȕ�����܂�4�j�B
Q3 �t���C���������������҂ւ̉^���Ö@�A����̃^�C�~���O����e���ǂ�����Č��߂܂����H
�t���C��������Ƃ킩������A�^���Ö@�ƐH���Ö@���������܂��B
�^���Ö@�ɂ��ẮA�܂��g�̊����ʂ��ቺ���Ă��Ȃ������`�F�b�N���܂��B
�Ƃɕ��������Ă��Ȃ����A�ƂŐQ�Ă��鎞�Ԃ������Ȃ��������₵�A���Ă͂܂�ꍇ�͍��ʂ܂��͉�ʂ̎��Ԃ�Z�����A�O�o�̋@��𑝂₷�悤�ɏ��������邱�Ƃ���ł��B
�t���C����ŗL���Ƃ���Ă���̂��A���W�X�^���X�^���Ƒ��v�f�̉^���ł��B
���W�X�^���X�^���͕��ׂ������ċؗ̓g���[�j���O���s�����̂ł��B
�s�����̉^�������A���ی��ŗ��p�\�ȃf�C�P�A�A�W���ł̃}�V���g���[�j���O�A�֎q���g���ẴX�N���b�g�A���R�g���A���K�A���Ɍ��Ȃǂ�����A�G���S���[�^�[�␅�����s�Ȃǂ����W�X�^���X�^���̗v�f������܂��B
�����͏��Ȃ��Ƃ��T2��ȏ�s�����Ƃ����߂Ă��܂��B
���v�f�̉^���́A���W�X�^���X�^�����ł��Ȃ��t���C���̍���҂ɑ��āA�X�g���b�`�^������n�܂�A�y�x�̃��W�X�^���X�^���A�o�����X�^���A�L�_�f�^����g�ݍ��킹�āA���W�X�^���X�^���̕��ׂ�傫�����Ă����^���ł��B���̑��v�f�̉^�����g�̋@�\�����߁A�t���C���i�s�\�h�ɗL���ł���Ƃ���Ă��܂��B
Q4 �t���C���������������҂ւ̐H���Ö@�A�G�l���M�[�A�b�v�̃R�c��t�@�\�ቺ��ł̑Ή��������Ă�������
�t���C�����l�������H���Ö@�͏\���ȃG�l���M�[�ʂ��m�ۂ��A�^���p�N���̐ێ�𑝂₷���Ƃ��|�C���g�ł��B
���B�h�{��ӊw��iESPEN�j�ł͍���҂̋ؓ��̗ʂƋ@�\���ێ����邽�߂ɂ͎��̏d�����菭�Ȃ��Ƃ�1.0�`1.2��/���̃^���p�N�����Ƃ邱�Ƃ���������Ă��܂�5)�B
�܂�A�̏d60�s�̐l��70g/���̃^���p�N���ێ悪�K�v�ɂȂ�܂��B
�t���C���̂悤�Ȓ�h�{�܂��͒�h�{���X�N������ꍇ�ɂ́A����ɑ����A�̏d������1.2�`1.5��/���̃^���p�N�����Ƃ邱�Ƃ����߂��܂��B
�t���C��������ꍇ�A�t��3���܂ł̓^���p�N�����\���ɂƂ�A�t��4���ł͕a��ɂ���Čʂɔ��f����̂������Ǝv���܂��B
�t�@�\�����̑��x�������ꍇ�⍂�������ǂ̏ꍇ�̓^���p�N��������D�悵�A�̏d�����A�ؗ͒ቺ�ȂǂŃt���C�����i�s���₷����Ԃ̏ꍇ�̓^���p�N���ێ�𑝂₷���Ƃ�D�悳���Ă͂ǂ����ƍl���Ă��܂��B
����҂͓����Ƃ邱�Ƃ����ȏꍇ������̂ŁA���A�����i�A���A�哤���i�Ȃǂ�g�ݍ��킹�ĂƂ邱�Ƃ����߂܂��B
�܂��A�^���p�N���̒��ł����Ƀ��C�V���̑����H�i�A�Ⴆ�u�����\�[�Z�[�W����i������v�Ƃ����������������̂ł͂Ȃ��ł��傤���B
���H�Ń^���p�N����K���Ƃ�悤�ɂ���ƁA1���̐ێ�ʂ𑝂₷���ƂɂȂ���܂��B
�G�l���M�[�ʂ͏]���A����҂͑̏d×25�`30kcal�Ƃ��Čv�Z���邱�Ƃ����������Ǝv���܂����A
�t���C���\�h���l�����ꍇ�A�̏d������30�`35kcal�Ƃ��ď\���ȃG�l���M�[�ʂ��m�ۂ��A�ɒ[�ȃG�l���M�[����������邱�Ƃ���ł��B�Ⴆ�Α̏d50�s�̏����ł́A1,600kcal�̐H���ƂȂ�܂��B
Q5 �t���C���������������A�a���҂ւ̖Ö@�A�l�����ׂ��|�C���g�́H
�t���C�������铜�A�a���҂̖Ö@�̃|�C���g��
1�j�ጌ���Ȃǂ̗L�Q���ۂ̃��X�N�����炷�悤�ȑI��������
2�j�t���C���̌����ƂȂ镹�������̎��Â��s��
3�j����A�h�q�A�����X�ቺ�̑�𗧂Ă�
���Ƃł��B
���ɏd�ǒጌ���ɂ͒��ӂ��K�v�ŁA�t���C�������łȂ��F�m�@�\��Q�A�]�|�E���܁AADL�ቺ�A����ԁAQOL�ቺ�ɂȂ���\��������܂��B
���������āA�t���C���̊��҂ł͒ጌ�����N�����ɂ�����܂𒆐S�Ƃ������Â��s���܂��B
���g�z���~����DPP-4�j�Q��Ȃǂ��܂��g�p���܂��B
SU����g�p����ꍇ�́A�ł��邾�����ʁA�Ⴆ�O���N���W�h10�`20�r/���Ŏg�p���܂��B
�t���C���̊��҂ł́A�̏d����������������SGLT2�j�Q��⍂�p�ʂ̃��g�z���~���̎g�p�ɂ͒��ӂ�v���܂��B
���ɐt�@�\�͒���I��eGFR�ŕ]�����A���ʂɉ����āA���g�z���~����SU��̗p�ʂ�����K�v������܂��BSU���eGFR45mL/��/1.73m2�����Ō��ʁAeGFR30mL/��/1.73m2�����Œ��~���܂��B
�t���C���̓��A�a���҂͐S�s�S�ACOPD�APAD�ȂǕ����̕���������L���Ă��邱�Ƃ������A���ꂪ�t���C���̌����ƂȂ��Ă���ꍇ������܂��B
���������āA�t���C���̌����ƂȂ鎾�������Â��邱�Ƃ���ł��B
�S�@�\�A�ċz�@�\�A���s�@�\�������ł����P���邱�Ƃ��A�t���C���̐i�s�h�~�ɂȂ���܂��B
�܂��A�y�x�̔F�m�@�\��Q�����Ƃ����Ȃ��Ȃ��A����A�h�q�A�����X�̒ቺ���������₷���Ȃ�܂��B
���ܕ��p�����ƂȂ�܂��B���҂͑o�����̊W������ƍl�����Ă���A���������̑�����^���Ö@�̕s�\�����Ȃǂ����ܕ��p�̌����ƂȂ肦�܂����A���ܕ��p���t���C���ɂȂ���\��������܂��B
���������āA�����������҂ł͎��Â̒P�������s�����Ƃ��K�v�ł��B
�������炷���Ƃ����łȂ��A��������炷���Ƃ╞��̃^�C�~���O�ꂷ�邱�Ƃ��P�����̎�i�Ƃ��ďd�v�ł��B
�Ⴆ�A��-GI��O���j�h����g�p����ꍇ�ɂ́A���ׂĂ̓������H���O�ɓ��ꂷ��悤�ɂ��Ă��܂��B
ADL�ቺ��F�m�ǂ�����ꍇ�ɂ́A�d�ǒጌ���̃��X�N�������̂ŁA���ʁE������l�����ׂ��ꍇ������܂��B
Q6 ���ɂǂ̂悤�Ȏ��Ï�̒��ӓ_������܂����H
�t���C�������銳�҂ł́A�F�m�@�\��Q�A��i�IADL�ቺ�A�g�̊����ʒቺ�A����ԁA��h�{�A����A�h�q�A�����X�ቺ�A�Љ�I�T�|�[�g�s���Ȃǂ��Ă���ꍇ�����Ȃ�����܂���B
���������āA��Ԃ��I�ɕ]���ł���CGA���s���A���̌��ʂɊ�Â��A�^��/�H��/�Ö@�����łȂ��A�Љ�I�T�|�[�g���s�����Ƃ���ɂȂ�܂��B
���ی���\�����A�v���ƔF�肳���A�f�C�P�A�Ȃǂ̃T�[�r�X���邱�Ƃ��ł��܂��B
�F�肳��Ȃ��ꍇ�ł��A�V�l��A�n��̍s���A�u����Ȃǂ̎Љ�Q���𑣂��āA���������h�����Ƃ��Љ�I�ȃt���C����h�����߂ɏd�v���ƍl���Ă��܂��B
�Q�l����
1�j Satake S, et al.Geriatr Gerontol Int.2016;16:709-715.
2�j Hanlon, et al. Lancet Public Health. 2018 Jun 13. [Epub ahead of print]
3�j Wong E et al. Lancet Diabetes Endocrinol. 2013 ;1: 106–14.
4�j Hubbard RE, et al. Diabet Med. 2010 ;27:603-606.
5�j Deutz NE, et al.Clin Nutr 2014;33:929-936.
6�j Kalyani RR, et al. J Am Geriatr Soc. 2012;60:1701-7.
7�j Park SW et al. Diabetes. 2006;55:1813-8.
8�j Yau RK, et al. Diabetes Care. 2013;36:3985-91.
9�j Schneider AL et al. Diabetes Care. 2013;36:1153-8.
��5��@���A�a���҂ƃt���C���EADL�y����ғ��A�a�f�ẪR�c�z
CareNet ���J���F2019/01/15
�r�� �� ( ���炫 ���� ) ��
�����s���N������ÃZ���^�[ ���A�a�E��ӁE��������� ���ȑ�������
J-CLEAR�]�c��
Q1 ���ہA���A�a���҂łǂ̂悤�Ƀt���C����]�����܂����H
����A�a���҂ł̓t���C���E�T���R�y�j�A�A��i�I/��{�IADL�A���́A���͂Ȃǂ̐g�̋@�\��]�����邱�Ƃ���ł��B
���̒��ŁA�t���C���͗v���ɂȂ邱�Ƃ�h���Ƃ����Ӗ��ŏd�v�ȕ]�����ڂ�1�ł��傤�B
�t���C���͉���ɔ����ė\���\���ቺ���A�X�g���X�ɂ���ėv���⎀�S�Ɋׂ�₷����Ԃƒ�`����܂��i�}�P�j�B

�{�M�ł̓t���C���͌��N�Ɨv���̒��Ԃ̏�ԂƂ���Ă��܂����A�C�O�ł͗v�����܂ޏꍇ������܂��B
�^����H������ɂ���Ĉꕔ���N�ȏ�Ԃɖ߂�ꍇ������Ƃ����t�����A�t���C���̓����ł��B
����1�̑傫�ȓ����͑��ʐ��ŁA�g�̓I�t���C�������łȂ��A�F�m�@�\�ቺ�₤�Ȃǂ̐��_�E�S���I�t���C���A��������Ȃǂ̎Љ�I�t���C�����܂߂��L���Ӗ��ŁA�t���C����]�����邱�Ƃ���ł��B
�t���C���ɂ͂��܂��܂Ȏw�W������܂����A�����ł͑傫�������ĂR�̃^�C�v���Љ�܂��B
1�ڂ͐g�̓I�t���C���ŁA�]���@�Ƃ���CHS�������܂��B
���̊��L.P.Fried�炪�������̂ŁA�̏d�����A��J���A�ؗ͒ቺ�A�g�̊����ʒቺ�A���s���x�ቺ��5���ڂ̂���3���ڈȏ㓖�Ă͂܂�ꍇ���t���C���Ƃ��܂��B
�̏d�����͒�h�{�A�ؗ͒ቺ�ƕ��s���x�ቺ�̓T���R�y�j�A�̏Ǐ�Ȃ̂ŁAFried��ɂ��g�̓I�t���C���́A��h�{��T���R�y�j�A���܂ފT�O�Ƃ������܂��B
�{�M�ł�CHS��̂��ꂼ��̍��ڂ̃J�b�g�I�t�l�⎿����C������J-CHS�������܂��i�\�P�j�B

2�ڂ�deficit accumulation model�i��Q�~�σ��f��)�ɂ��t���C���ŁA����҂ɑ����@�\��Q�⎾���̏W�ςɂ���Ē�`����܂��B
36���ڂ���Ȃ�Frailty Index����\�I�Ȋ�ł��B
��Q�������d�Ȃ邱�Ƃŗ\���\���ቺ���A���S�̃��X�N���傫���Ȃ�Ƃ����l���Ɋ�Â��č쐬����Ă��܂����A���ڐ��������A�Տ��I�Ɏg���ɂ����̂�����ł��B
3�ڂ͍���ґ����@�\�]���iCGA�j�Ɋ�Â����t���C���ł���A�g�̋@�\�A�F�m�@�\�A����ԁA��h�{�Ȃǂ𑍍��I�ɕ]���������ʂɊ�Â��ĕ]��������̂ł��B
�{�M�ł͉��\�h���f�Ŏg�p����Ă���u��{�`�F�b�N���X�g�v��CGA�Ɋ�Â����t���C���Ƃ�����ł��傤�B
ADL�A�T���R�y�j�A�֘A�A��h�{�A���o�@�\�A��������A�F�m�A���Ȃǂ�25���ڂ�]�����A8���ڈȏ㓖�Ă͂܂�ꍇ���t���C���Ƃ��܂�1)�i�\�Q�j�B

�O���ʉ@�̍���A�a���҂ł܂��ȒP�Ɏ��{�ł���̂�J-CHS�ł��傤�B
��{�`�F�b�N���X�g���s�����Ƃ��ł���A�L���Ӗ��Ńt���C���̕]�����ł��܂��B
��{�`�F�b�N���X�g���s���̂�����ꍇ�ɂ�DASC-8���s���āA�i����ғ��A�a�̌����R���g���[���ڕW�ɂ�����j�J�e�S���[II�̊��҂�ΏۂɃt���C������s���Ƃ������@������܂��B
Q2 ���A�a�ƃt���C���EADL�ቺ�̊W�A�댯���q�́H
���A�a���҂́A����҂����łȂ����N�҂ł��t���C�����������₷�����Ƃ��킩���Ă��܂��B
���A�a���Ȃ��l�Ɣ�ׂāA���A�a���҂ł̓t���C���̃��X�N����5�{�A�v���t���C���̃��X�N����2.3�{�ƕ���Ă��܂�2)�B�܂��A���A�a���҂ł͎�i�IADL�ቺ��1.65�{�A��{�IADL�ቺ��1.82�{�������₷���Ƃ������^��͌��ʂ�����܂�3)�B
����A�a���҂ł́A���ɍ������A�d�ǒጌ���A�����d���������̍������t���C���̊댯���q�Ƃ��ďd�v�ł��BHbA1c 8.0���ȏ�̊��҂̓t���C���A���s���x�ቺ�A�]�|�A���܂��N�����₷���Ȃ�܂��i�}�Q�j�B
![�}2�������̓t���C���]�|����.jpg](/mappei/file/E59BB32E9AB98E8A180E7B396E381AFE38395E383ACE382A4E383ABE8BBA2E58092E9AAA8E68A98-thumbnail2.jpg)
������d�v�Ȃ��Ƃ́A���A�a�Ƀt���C������������Ǝ��S���X�N���傫���Ȃ邱�Ƃł��B
�_�������ďd�Ǔx���]���ł���t���C���ł́A�t���C�����d�ǂł���قǎ��S�̃��X�N�����܂邱�Ƃ��킩���Ă��܂��B
�p���̒����ł́A���A�a�Ƀt���C���������������҂ł͕��ϗ]���i�����l�j��23�����Ƃ����A�ɒ[�ȕ�����܂�4�j�B
Q3 �t���C���������������҂ւ̉^���Ö@�A����̃^�C�~���O����e���ǂ�����Č��߂܂����H
�t���C��������Ƃ킩������A�^���Ö@�ƐH���Ö@���������܂��B
�^���Ö@�ɂ��ẮA�܂��g�̊����ʂ��ቺ���Ă��Ȃ������`�F�b�N���܂��B
�Ƃɕ��������Ă��Ȃ����A�ƂŐQ�Ă��鎞�Ԃ������Ȃ��������₵�A���Ă͂܂�ꍇ�͍��ʂ܂��͉�ʂ̎��Ԃ�Z�����A�O�o�̋@��𑝂₷�悤�ɏ��������邱�Ƃ���ł��B
�t���C����ŗL���Ƃ���Ă���̂��A���W�X�^���X�^���Ƒ��v�f�̉^���ł��B
���W�X�^���X�^���͕��ׂ������ċؗ̓g���[�j���O���s�����̂ł��B
�s�����̉^�������A���ی��ŗ��p�\�ȃf�C�P�A�A�W���ł̃}�V���g���[�j���O�A�֎q���g���ẴX�N���b�g�A���R�g���A���K�A���Ɍ��Ȃǂ�����A�G���S���[�^�[�␅�����s�Ȃǂ����W�X�^���X�^���̗v�f������܂��B
�����͏��Ȃ��Ƃ��T2��ȏ�s�����Ƃ����߂Ă��܂��B
���v�f�̉^���́A���W�X�^���X�^�����ł��Ȃ��t���C���̍���҂ɑ��āA�X�g���b�`�^������n�܂�A�y�x�̃��W�X�^���X�^���A�o�����X�^���A�L�_�f�^����g�ݍ��킹�āA���W�X�^���X�^���̕��ׂ�傫�����Ă����^���ł��B���̑��v�f�̉^�����g�̋@�\�����߁A�t���C���i�s�\�h�ɗL���ł���Ƃ���Ă��܂��B
Q4 �t���C���������������҂ւ̐H���Ö@�A�G�l���M�[�A�b�v�̃R�c��t�@�\�ቺ��ł̑Ή��������Ă�������
�t���C�����l�������H���Ö@�͏\���ȃG�l���M�[�ʂ��m�ۂ��A�^���p�N���̐ێ�𑝂₷���Ƃ��|�C���g�ł��B
���B�h�{��ӊw��iESPEN�j�ł͍���҂̋ؓ��̗ʂƋ@�\���ێ����邽�߂ɂ͎��̏d�����菭�Ȃ��Ƃ�1.0�`1.2��/���̃^���p�N�����Ƃ邱�Ƃ���������Ă��܂�5)�B
�܂�A�̏d60�s�̐l��70g/���̃^���p�N���ێ悪�K�v�ɂȂ�܂��B
�t���C���̂悤�Ȓ�h�{�܂��͒�h�{���X�N������ꍇ�ɂ́A����ɑ����A�̏d������1.2�`1.5��/���̃^���p�N�����Ƃ邱�Ƃ����߂��܂��B
�t���C��������ꍇ�A�t��3���܂ł̓^���p�N�����\���ɂƂ�A�t��4���ł͕a��ɂ���Čʂɔ��f����̂������Ǝv���܂��B
�t�@�\�����̑��x�������ꍇ�⍂�������ǂ̏ꍇ�̓^���p�N��������D�悵�A�̏d�����A�ؗ͒ቺ�ȂǂŃt���C�����i�s���₷����Ԃ̏ꍇ�̓^���p�N���ێ�𑝂₷���Ƃ�D�悳���Ă͂ǂ����ƍl���Ă��܂��B
����҂͓����Ƃ邱�Ƃ����ȏꍇ������̂ŁA���A�����i�A���A�哤���i�Ȃǂ�g�ݍ��킹�ĂƂ邱�Ƃ����߂܂��B
�܂��A�^���p�N���̒��ł����Ƀ��C�V���̑����H�i�A�Ⴆ�u�����\�[�Z�[�W����i������v�Ƃ����������������̂ł͂Ȃ��ł��傤���B
���H�Ń^���p�N����K���Ƃ�悤�ɂ���ƁA1���̐ێ�ʂ𑝂₷���ƂɂȂ���܂��B
�G�l���M�[�ʂ͏]���A����҂͑̏d×25�`30kcal�Ƃ��Čv�Z���邱�Ƃ����������Ǝv���܂����A
�t���C���\�h���l�����ꍇ�A�̏d������30�`35kcal�Ƃ��ď\���ȃG�l���M�[�ʂ��m�ۂ��A�ɒ[�ȃG�l���M�[����������邱�Ƃ���ł��B�Ⴆ�Α̏d50�s�̏����ł́A1,600kcal�̐H���ƂȂ�܂��B
Q5 �t���C���������������A�a���҂ւ̖Ö@�A�l�����ׂ��|�C���g�́H
�t���C�������铜�A�a���҂̖Ö@�̃|�C���g��
1�j�ጌ���Ȃǂ̗L�Q���ۂ̃��X�N�����炷�悤�ȑI��������
2�j�t���C���̌����ƂȂ镹�������̎��Â��s��
3�j����A�h�q�A�����X�ቺ�̑�𗧂Ă�
���Ƃł��B
���ɏd�ǒጌ���ɂ͒��ӂ��K�v�ŁA�t���C�������łȂ��F�m�@�\��Q�A�]�|�E���܁AADL�ቺ�A����ԁAQOL�ቺ�ɂȂ���\��������܂��B
���������āA�t���C���̊��҂ł͒ጌ�����N�����ɂ�����܂𒆐S�Ƃ������Â��s���܂��B
���g�z���~����DPP-4�j�Q��Ȃǂ��܂��g�p���܂��B
SU����g�p����ꍇ�́A�ł��邾�����ʁA�Ⴆ�O���N���W�h10�`20�r/���Ŏg�p���܂��B
�t���C���̊��҂ł́A�̏d����������������SGLT2�j�Q��⍂�p�ʂ̃��g�z���~���̎g�p�ɂ͒��ӂ�v���܂��B
���ɐt�@�\�͒���I��eGFR�ŕ]�����A���ʂɉ����āA���g�z���~����SU��̗p�ʂ�����K�v������܂��BSU���eGFR45mL/��/1.73m2�����Ō��ʁAeGFR30mL/��/1.73m2�����Œ��~���܂��B
�t���C���̓��A�a���҂͐S�s�S�ACOPD�APAD�ȂǕ����̕���������L���Ă��邱�Ƃ������A���ꂪ�t���C���̌����ƂȂ��Ă���ꍇ������܂��B
���������āA�t���C���̌����ƂȂ鎾�������Â��邱�Ƃ���ł��B
�S�@�\�A�ċz�@�\�A���s�@�\�������ł����P���邱�Ƃ��A�t���C���̐i�s�h�~�ɂȂ���܂��B
�܂��A�y�x�̔F�m�@�\��Q�����Ƃ����Ȃ��Ȃ��A����A�h�q�A�����X�̒ቺ���������₷���Ȃ�܂��B
���ܕ��p�����ƂȂ�܂��B���҂͑o�����̊W������ƍl�����Ă���A���������̑�����^���Ö@�̕s�\�����Ȃǂ����ܕ��p�̌����ƂȂ肦�܂����A���ܕ��p���t���C���ɂȂ���\��������܂��B
���������āA�����������҂ł͎��Â̒P�������s�����Ƃ��K�v�ł��B
�������炷���Ƃ����łȂ��A��������炷���Ƃ╞��̃^�C�~���O�ꂷ�邱�Ƃ��P�����̎�i�Ƃ��ďd�v�ł��B
�Ⴆ�A��-GI��O���j�h����g�p����ꍇ�ɂ́A���ׂĂ̓������H���O�ɓ��ꂷ��悤�ɂ��Ă��܂��B
ADL�ቺ��F�m�ǂ�����ꍇ�ɂ́A�d�ǒጌ���̃��X�N�������̂ŁA���ʁE������l�����ׂ��ꍇ������܂��B
Q6 ���ɂǂ̂悤�Ȏ��Ï�̒��ӓ_������܂����H
�t���C�������銳�҂ł́A�F�m�@�\��Q�A��i�IADL�ቺ�A�g�̊����ʒቺ�A����ԁA��h�{�A����A�h�q�A�����X�ቺ�A�Љ�I�T�|�[�g�s���Ȃǂ��Ă���ꍇ�����Ȃ�����܂���B
���������āA��Ԃ��I�ɕ]���ł���CGA���s���A���̌��ʂɊ�Â��A�^��/�H��/�Ö@�����łȂ��A�Љ�I�T�|�[�g���s�����Ƃ���ɂȂ�܂��B
���ی���\�����A�v���ƔF�肳���A�f�C�P�A�Ȃǂ̃T�[�r�X���邱�Ƃ��ł��܂��B
�F�肳��Ȃ��ꍇ�ł��A�V�l��A�n��̍s���A�u����Ȃǂ̎Љ�Q���𑣂��āA���������h�����Ƃ��Љ�I�ȃt���C����h�����߂ɏd�v���ƍl���Ă��܂��B
�Q�l����
1�j Satake S, et al.Geriatr Gerontol Int.2016;16:709-715.
2�j Hanlon, et al. Lancet Public Health. 2018 Jun 13. [Epub ahead of print]
3�j Wong E et al. Lancet Diabetes Endocrinol. 2013 ;1: 106–14.
4�j Hubbard RE, et al. Diabet Med. 2010 ;27:603-606.
5�j Deutz NE, et al.Clin Nutr 2014;33:929-936.
6�j Kalyani RR, et al. J Am Geriatr Soc. 2012;60:1701-7.
7�j Park SW et al. Diabetes. 2006;55:1813-8.
8�j Yau RK, et al. Diabetes Care. 2013;36:3985-91.
9�j Schneider AL et al. Diabetes Care. 2013;36:1153-8.
���̋L���ւ̃R�����g
�R�����g������
���̋L���ւ̃g���b�N�o�b�NURL
https://fanblogs.jp/tb/8477748
���u���O�I�[�i�[�����F�����g���b�N�o�b�N�̂ݕ\������܂��B
���̋L���ւ̃g���b�N�o�b�N